Covid-19: Ya hay vacunas y funcionan pero ¿qué pasa con los medicamentos?
María Mercedes Jiménez Sarmiento, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC); Matilde Cañelles López, Instituto de Filosofía (IFS-CSIC) y Nuria Eugenia Campillo, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC)
Día a día, observamos que las vacunas contra la COVID-19 tienen el potencial de disminuir drásticamente la gravedad de la enfermedad. Pero también nos damos cuenta de que la vacunación será un proceso largo, que se producen deficiencias en el suministro de vacunas, y que asistimos a una desigualdad y retraso en la mayoría de los países. Tampoco podemos olvidar que, mientras tanto, pueden aparecer nuevas variantes y que aún desconocemos la duración de la inmunidad adquirida.
Además, aunque de momento consigamos atajar al SARS-CoV-2, podrían surgir periódicamente brotes de la enfermedad (como ocurre con el ébola). Por otra parte, no podemos dejar de lado a millones de personas que por distintos motivos no pueden ser vacunadas, por tener el sistema inmune comprometido, o porque no consiguen desarrollar inmunidad contra la COVID-19 ni siquiera con la pauta completa de vacunación.
La solución a estos problemas pasaría por encontrar un tratamiento definitivo de la enfermedad. Idealmente debería ser de fácil acceso y aplicación (oral, por ejemplo) y eliminar o limitar la transmisión viral. Puestos a pedir…
¿Qué es el reposicionamiento de fármacos?
El proceso tradicional de desarrollo de un medicamento es un proceso complejo que conlleva tiempos muy largos y grandes inversiones. Por eso, desde el comienzo, el primer recurso fue utilizar fármacos ya establecidos en cuanto a rapidez y seguridad que pudieran servir para combatir una nueva patología como la COVID-19. Lo que se conoce como reposicionamiento de fármacos.
El proceso de reposicionamiento ayuda a acelerar el desarrollo de un fármaco ya que se eliminan varias etapas. Por ejemplo, los estudios preclínicos que evalúan la seguridad de los fármacos previos a la aprobación por parte de las agencias reguladoras para pasar a los estudios clínicos. Además, cuando un medicamento ya está en el mercado y se utiliza habitualmente para otras enfermedades, se puede eliminar la Fase I de los ensayos clínicos, ahorrando mucho tiempo, esfuerzo y dinero.
Acortar el tiempo es siempre importante, pero en situaciones como la pandemia actual que estamos viviendo es de enorme necesidad.
Los tratamientos actuales son reposicionados, pero no son definitivos.
A pesar del gran esfuerzo realizado, las opciones de terapia para la COVID-19 siguen siendo bastante limitadas. Los médicos aplican corticosteroides (dexametasona) y remdesivir (compuesto antiviral contra el ébola) por vía intravenosa para los casos críticos.
Los primeros tratamientos con hidroxicloroquina, lopinavir e interferón, ivermectina, aplidina, colchicina o antitumorales, a los que hay que añadir los anticuerpos monoclonales, y los más de 300 ensayos clínicos registrados no han mostrado resultados definitivos. Las conclusiones de los ensayos multicéntricos internacionales Solidarity (OMS) y Recovery (Reino Unido) han constatado evidencias de mejoría a favor únicamente de la dexametasona.
¿Estamos ante un fracaso? No exactamente.
La comunidad científica sigue investigando sobre tratamientos específicos dirigidos directamente contra el SARS-CoV-2 y también buscando en quimiotecas (colecciones) de compuestos tanto conocidas (como la quimioteca de fármacos de la FDA) como quimiotecas diseñadas.
El escaso éxito entre candidatos a fármacos de alto valor que se reutilizan para la infección por SARS-CoV-2 refleja la escasez de compuestos antivirales y antiinfecciosos avanzados y aprobados, y destaca aún más la necesidad de investigar en nuevos fármacos de este tipo.

¿Cómo se han encontrado otros potenciales candidatos?
A partir de miles de moléculas conocidas, los investigadores tratan de encontrar una aguja en un pajar: un compuesto para el que se demuestre y valide una actividad específica que impida el desarrollo de la enfermedad.
Muy recientemente, un grupo de investigadores del Scripps Research Institute (La Jolla, USA) ha desarrollado una metodología de cribado fenotípico masivo con el fin de identificar fármacos ya conocidos.
Utilizan dos quimiotecas de compuestos: una “quimioteca piloto” de 148 fármacos conocidos con potencial actividad coronavírica y la quimioteca ReFRAME (Reporpousing, Focused Rescue and Accelarated MedChem) con más de 12.000 fármacos. Esta útima colección está formada por tres bases de datos de medicamentos comerciales ampliamente utilizadas (Clarivate Integrity, GVK Excelra GoStar y Citeline Pharmaprojects), junto con un gran grupo de compuestos extraídos de patentes que se han utilizado en humanos ¡Más de 12.000 moléculas!
La búsqueda de la aguja en el pajar –o protocolo de cribado, como se denomina en jerga científica– está formada por diferentes ensayos experimentales que se visualizan en la Figura 1.
Los dos primeros filtros consisten en dos ensayos de infección en células cultivadas: células HeLa que expresan el receptor ACE2 del SARS-CoV-2 y células epiteliales pulmonares Calu-3 donde se expresan además del receptor ACE2, el TMPRSS2.
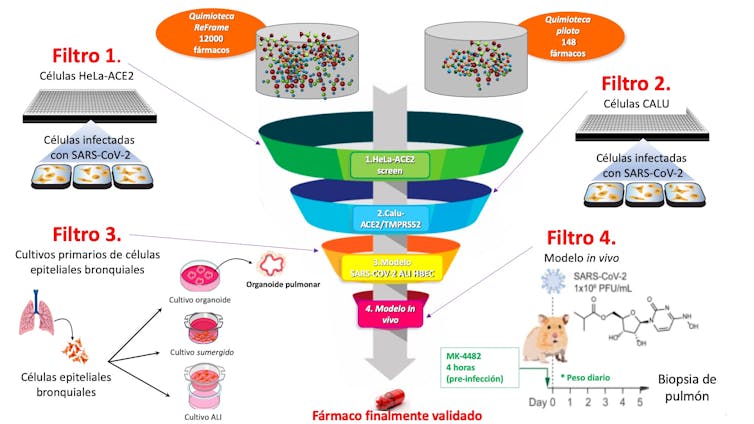
A partir de probar los 12.000 compuestos de las dos quimiotecas se identificaron 49 (en HeLa-ACE2) y 41 (en Calu-3) compuestos capaces de inhibir selectivamente la replicación del SARS-CoV-2. Menos de un 1% de las moléculas del comienzo.
Entre los compuestos mas prometedores, los investigadores identificaron de la “químioteca piloto” los antivirales nelfinavir y el profármaco MK-4482. Ambos reducen la replicación del SARS-CoV-2 en cultivos primarios de células epiteliales bronquiales humanas (filtro 3). Estos dos compuestos son medicamentos conocidos, por lo que presentan un buen perfil de absorción, actividad y seguridad en humanos.
Posteriormente, se estudió el compuesto MK-4482 en un modelo animal (filtro 4), comprobando que bloquea eficazmente la infección por SARS-CoV-2.
Actualmente se esta estudiando la eficacia del compuesto MK-4482 en ensayos clínicos II/III (Ridgeback Biotherapeutics and Merck) para evaluar la seguridad y la eficacia. Menos de 0,01% con respecto a las moléculas de partida.
Las vacunas nos han permitido respirar y ver la luz al final del túnel, pero no hay que olvidar que se necesitan tratamientos farmacológicos eficaces para tratar la COVID-19.
Por parte de la comunidad científica se está haciendo un serio esfuerzo por identificar fármacos tanto de reposicionamiento como de nueva generación. Lo importante es conseguir un arsenal de antivirales capaces de luchar contra este virus. Y si de paso nos sirven para otros futuros, pues mejor que mejor.![]()
María Mercedes Jiménez Sarmiento, Científica del CSIC. Bioquímica de Sistemas de la división bacteriana. Comunicadora científica, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC); Matilde Cañelles López, Investigadora Científica. Ciencia, Tecnología y Sociedad, Instituto de Filosofía (IFS-CSIC) y Nuria Eugenia Campillo, Científico Titular. Medicinal Chemistry, Centro de Investigaciones Biológicas Margarita Salas (CIB – CSIC)
Este artículo fue publicado originalmente en The Conversation. Lea el original.
